Geminální diolyEdit
Geminální diol má dvě hydroxylové skupiny vázané na stejný atom. Tyto druhy vznikají hydratací karbonylových sloučenin. Hydratace je obvykle nepříznivá, ale významnou výjimkou je formaldehyd, který ve vodě existuje v rovnováze s methanediolem H2C(OH)2 . Dalším příkladem je (F3C)2C(OH)2, hydratovaná forma hexafluoroacetonu. Mnoho gem-diolů podléhá další kondenzaci za vzniku dimerních a oligomerních derivátů. Tato reakce se týká glyoxalu a příbuzných aldehydů.
Vicinální diolyEdit
Ve vicinálním diolu zaujímají dvě hydroxylové skupiny vicinální polohy, tj. jsou připojeny k sousedním atomům. Tyto sloučeniny se nazývají glykoly. Příkladem je 1,2-etandiol nebo ethylenglykol HO-(CH2)2-OH, běžná složka nemrznoucích směsí. Dalším příkladem je propan-1,2-diol neboli alfa propylenglykol, HO-CH2-CH(OH)-CH3, používaný v potravinářském a lékařském průmyslu a také jako relativně nejedovatý nemrznoucí výrobek.
V komerčním měřítku je hlavní cestou k vicinálním diolům hydrolýza epoxidů. Epoxidy se připravují epoxidací alkenů. Příklad v syntéze trans-cyklohexandiolu nebo mikroreaktorem:

Pro akademický výzkum a farmaceutické oblasti se vicinální dioly často vyrábějí oxidací alkenů, obvykle zředěným kyselým manganistanem draselným. Při použití alkalického manganistanu draselného(VII) dochází ke změně barvy z čiré tmavě fialové na jasně zelenou; kyselý manganistan draselný(VII) se mění na čirý bezbarvý. Podobně lze tetroxid osmia použít k oxidaci alkenů na vicinální dioly. Chemickou reakci zvanou Sharplessova asymetrická dihydroxylace lze použít k výrobě chirálních diolů z alkenů za použití osmátového činidla a chirálního katalyzátoru. Další metodou je Woodwardova cis-hydroxylace (cis diol) a příbuzná Prévostova reakce (anti diol), znázorněná níže, které obě využívají jód a stříbrnou sůl karboxylové kyseliny.
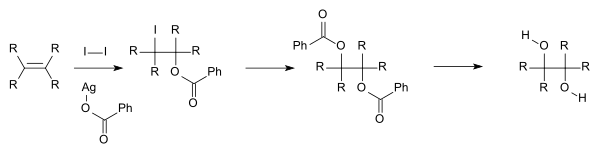
Dalšími cestami k vic-diolům jsou hydrogenace acyloinů a pinakolová spojovací reakce.
1,3-DiolyPříprava
1,3-Dioly se často průmyslově připravují aldolovou kondenzací ketonů s formaldehydem. Vzniklý karbonyl se redukuje Cannizzarovou reakcí nebo katalytickou hydrogenací:
RC(O)CH3 + CH2O → RC(O)CH2CH2OH RC(O)CH2CH2OH + H2 → RCH(OH)CH2CH2OH
Tímto způsobem se připravují 2,2-disubstituované propan-1,3-dioly. Příkladem je 2-methyl-2-propyl-1,3-propandiol a neopentylglykol.
1,3-dioly lze připravit hydratací α,β-nenasycených ketonů a aldehydů. Vzniklý ketoalkohol se hydrogenuje. Jiný způsob zahrnuje hydroformylaci epoxidů s následnou hydrogenací aldehydu. Tato metoda byla použita pro 1,3-propandiol z ethylenoxidu.
Specializovanější cesty k 1,3-diolům zahrnují reakci mezi alkenem a formaldehydem, Prinsovu reakci. 1,3-dioly lze vyrábět diastereoselektivně z odpovídajících β-hydroxy ketonů pomocí redukčních protokolů Evans-Saksena, Narasaka-Prasad nebo Evans-Tishchenko.
1,3-dioly se popisují jako syn nebo anti v závislosti na relativní stereochemii uhlíkových atomů nesoucích hydroxylové funkční skupiny. Zinkoforin je přírodní produkt, který obsahuje jak syn, tak anti 1,3-dioly.
1,4-, 1,5- a delší diolyUpravit
.