Geminal diolerRediger
En geminal diol har to hydroxylgrupper bundet til det samme atom. Disse arter opstår ved hydrering af carbonylforbindelserne. Hydreringen er normalt ugunstig, men en bemærkelsesværdig undtagelse er formaldehyd, som i vand eksisterer i ligevægt med metandiol H2C(OH)2. Et andet eksempel er (F3C)2C(OH)2, den hydrerede form af hexafluoroacetone. Mange gem-dioler undergår yderligere kondensation for at give dimeriske og oligomeriske derivater. Denne reaktion gælder for glyoxal og beslægtede aldehyder.
Vicinale diolerRediger
I en vicinal diol indtager de to hydroxylgrupper vicinale positioner, det vil sige, at de er knyttet til tilstødende atomer. Disse forbindelser kaldes glykoler. Som eksempler kan nævnes 1,2-ethandiol eller ethylenglycol HO-(CH2)2-OH, der er en almindelig bestanddel i frostsikringsmidler. Et andet eksempel er propan-1,2-diol eller alfa-propylenglycol, HO-CH2-CH(OH)-CH3, der anvendes i fødevare- og medicinalindustrien og er et relativt ugiftigt frostbeskyttelsesmiddel.
På kommerciel skala er den vigtigste vej til vicinale dioler hydrolysen af epoxider. Epoxiderne fremstilles ved epoxidering af alkenet. Et eksempel i syntesen af trans-cyclohexandiol eller ved mikroreaktor:

Til akademisk forskning og farmaceutiske områder fremstilles vicinale dioler ofte ved oxidation af alkener, sædvanligvis med fortyndet surt kaliumpermanganat. Ved anvendelse af alkalisk kaliummanganat(VII) sker der et farveskift fra klar dyblilla til klar grøn; surt kaliummanganat(VII) bliver klart farveløst. Osmiumtetroxid kan ligeledes anvendes til at oxidere alkener til vicinale dioler. Den kemiske reaktion kaldet Sharpless asymmetrisk dihydroxylering kan anvendes til at fremstille chirale dioler fra alkener ved hjælp af et osmatreagens og en chiral katalysator. En anden metode er Woodward-cis-hydroxyleringen (cis-diol) og den beslægtede Prévost-reaktion (anti-diol), som er afbildet nedenfor, og som begge anvender jod og sølvsaltet af en carboxylsyre.
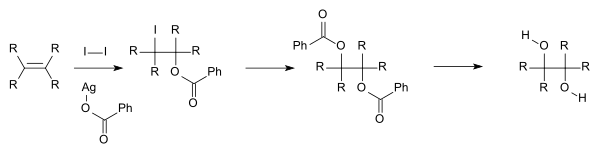
Andre veje til vic-dioler er hydrogenering af acyloiner og pinacol-koblingsreaktionen.
1,3-DiolerRediger
1,3-Dioler fremstilles ofte industrielt ved aldolkondensation af ketoner med formaldehyd. Den resulterende carbonyl reduceres ved hjælp af Cannizzaro-reaktionen eller ved katalytisk hydrogenering:
RC(O)CH3 + CH2O → RC(O)CH2CH2OH RC(O)CH2CH2OH + H2 → RCH(OH)CH2CH2OH
2,2-Disubstituerede propan-1,3-dioler fremstilles på denne måde. Som eksempler kan nævnes 2-methyl-2-propyl-1,3-propandiol og neopentylglycol.
1,3-dioler kan fremstilles ved hydrering af α,β-umættede ketoner og aldehyder. Den resulterende keto-alkohol hydrogeneres. En anden rute omfatter hydroformylering af epoxider efterfulgt af hydrogenering af aldehydet. Denne metode er blevet anvendt til 1,3-propandiol fra ethylenoxid.
Mere specialiserede ruter til 1,3-dioler involverer reaktionen mellem et alken og formaldehyd, Prins-reaktionen. 1,3-dioler kan fremstilles diastereoselektivt fra de tilsvarende β-hydroxyketoner ved hjælp af Evans-Saksena-, Narasaka-Prasad- eller Evans-Tishchenko-reduktionsprotokollerne.
1,3-dioler beskrives som syn eller anti afhængigt af de relative stereokemier af de kulstofatomer, der bærer de hydroxylfunktionelle grupper. Zinkophorin er et naturprodukt, der indeholder både syn- og anti-1,3-dioler.