GeminaldiolerRedigera
En geminaldiol har två hydroxylgrupper bundna till samma atom. Dessa arter uppstår genom hydrering av karbonylföreningarna. Hydreringen är vanligtvis ogynnsam, men ett anmärkningsvärt undantag är formaldehyd som i vatten existerar i jämvikt med metandiol H2C(OH)2. Ett annat exempel är (F3C)2C(OH)2, den hydratiserade formen av hexafluoroaceton. Många gem-dioler genomgår ytterligare kondensation för att ge dimeriska och oligomeriska derivat. Denna reaktion gäller för glyoxal och besläktade aldehyder.
Vicinala diolerRedigera
I en vicinal diol intar de två hydroxylgrupperna vicinala positioner, det vill säga de är knutna till intilliggande atomer. Dessa föreningar kallas glykoler. Som exempel kan nämnas 1,2-etandiol eller etylenglykol HO-(CH2)2-OH, en vanlig ingrediens i frostskyddsmedel. Ett annat exempel är propan-1,2-diol eller alfapropylenglykol, HO-CH2-CH(OH)-CH3, som används inom livsmedels- och läkemedelsindustrin samt som en relativt giftfri frostskyddsprodukt.
I kommersiell skala är den huvudsakliga vägen till vicinala dioler hydrolysen av epoxider. Epoxiderna framställs genom epoxidering av alkenen. Ett exempel i syntesen av trans-cyklohexandiol eller genom mikroreaktor:

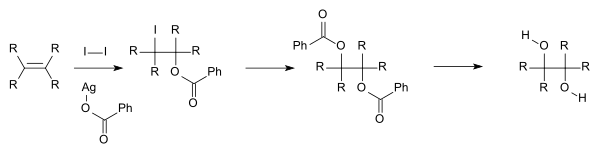
För akademisk forskning och farmaceutiska områden framställs vicinaldioler ofta genom oxidation av alkener, vanligen med utspädd sur kaliumpermanganat. Användning av alkaliskt kaliummanganat(VII) ger en färgförändring från klart djupt lila till klart grönt; surt kaliummanganat(VII) blir klart färglöst. Osmiumtetroxid kan på samma sätt användas för att oxidera alkener till vicinala dioler. Den kemiska reaktion som kallas Sharpless asymmetrisk dihydroxylering kan användas för att framställa chirala dioler från alkener med hjälp av ett osmatreagens och en chiral katalysator. En annan metod är Woodward cis-hydroxylering (cis-diol) och den besläktade Prévost-reaktionen (anti-diol), som beskrivs nedan, som båda använder jod och silversalt av en karboxylsyra.
Andra vägar till vic-dioler är hydrering av acyloiner och pinacolkopplingsreaktionen.
1,3-DiolerRedigera
1,3-Dioler framställs ofta industriellt genom aldolkondensation av ketoner med formaldehyd. Den resulterande karbonylen reduceras med hjälp av Cannizzaroreaktionen eller genom katalytisk hydrering:
RC(O)CH3 + CH2O → RC(O)CH2CH2OH RC(O)CH2CH2OH + H2 → RCH(OH)CH2CH2OH
2,2-Disubstituerade propan-1,3-dioler framställs på detta sätt. Som exempel kan nämnas 2-metyl-2-propyl-1,3-propandiol och neopentylglykol.
1,3-dioler kan framställas genom hydrering av α,β-omättade ketoner och aldehyder. Den resulterande ketoalkoholen hydreras. En annan väg innebär hydroformylering av epoxider följt av hydrering av aldehyden. Denna metod har använts för 1,3-propandiol från etylenoxid.
Mer specialiserade vägar till 1,3-dioler innefattar reaktionen mellan en alken och formaldehyd, Prins-reaktionen. 1,3-dioler kan framställas diastereoselektivt från motsvarande β-hydroxiketoner med hjälp av Evans-Saksena-, Narasaka-Prasad- eller Evans-Tishchenko-reduktionsprotokollet.
1,3-dioler beskrivs som syn- eller antidioler beroende på den relativa stereokemi som gäller för de kolatomer som bär de funktionella hydroxylgrupperna. Zinkophorin är en naturprodukt som innehåller både syn- och anti-1,3-dioler.